Neuroprotektion hos kritisk syge med potentielt forhøjet ICP
Neuroprotektionsfolder som selvstændig pdf
Udarbejdet af arbejdsgruppe under DASAIM og DSIT
Godkendt af DASAIM/DSIT februar 2021
Gyldig fra: Februar 2021
Revision senest: Februar 2025
Tovholder/Korrespondance:
Christian Overgaard-Steensen (Region Hovedstaden)
E-mail: christian.overgaard.steensen@regionh.dk.
Arbejdsgruppe/Referenter:
Christine Lodberg Hvas (Region Midt), Line Thorup (Region Midt), Jeppe Bove (Region Syd), KarenLise Welling (Region Hovedstaden), Jacob Madsen (Region Nord), Pernille Haure Christensen (Region Nord), Hans Fjeldsø-Nielsen (Region Sjælland), Susanne Andi Iversen (Region Sjælland), Vagn Eskesen (Neurokirurg), Sarah Hornshøj Pedersen (Neurokirurg), Klaus Hansen (Neurolog), Aase Bengård Andersen (Infektionsmediciner).
Interessekonflikter: Ingen i gruppen har meldt om interessekonflikter.
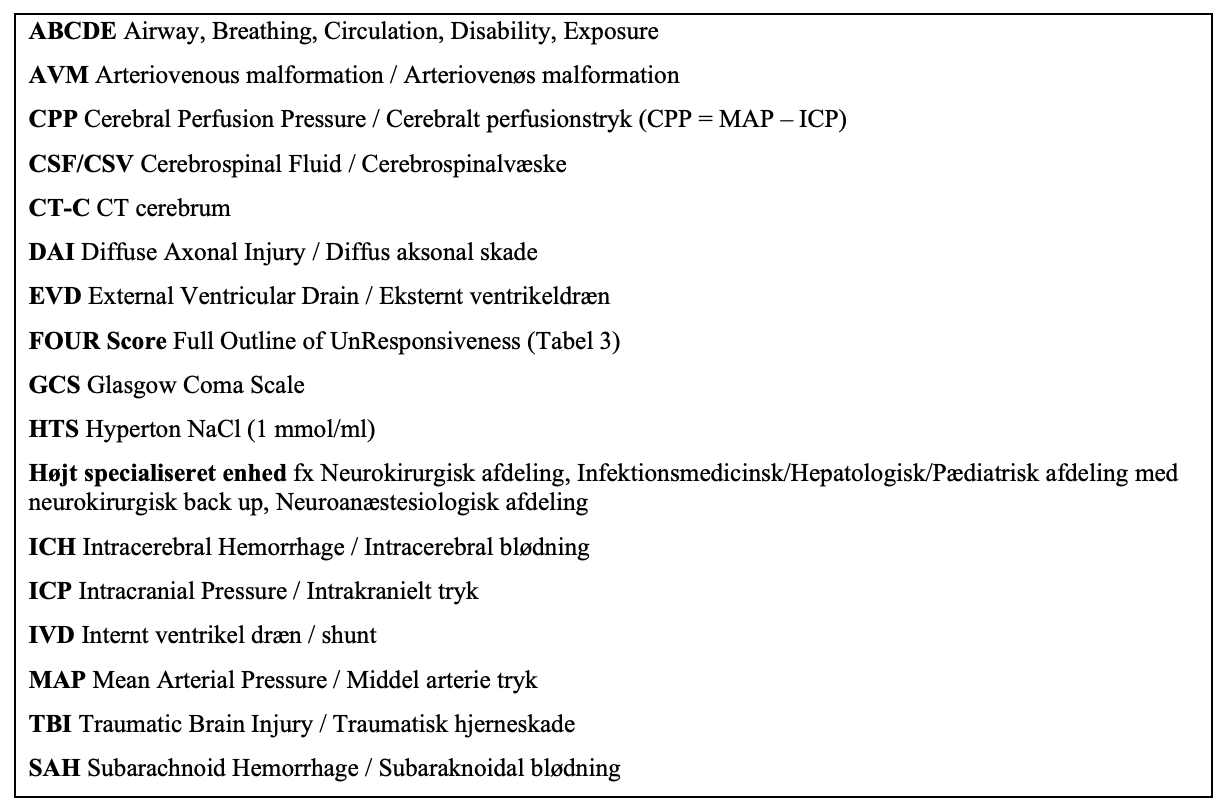
Forkortelser/definitioner
Indledning
Kritisk syge børn og voksne kan potentielt eller manifest have forhøjet intrakranielt tryk (ICP) med nedsat cerebralt perfusionstryk (CPP = MAP – ICP) (Tabel 1). Forhøjet ICP er associeret til dårligt outcome og kan forårsage inkarceration 1-3. Forhøjet ICP kan være til stede trods normal CT-scanning af cerebrum (CT-C)4 5 og en høj grad af opmærksomhed er afgørende for at undgå yderligere forværring. Neuroprotektiv behandling kræver praktisk viden om faktorer af betydning for ICP/CPP, erkendelse af tiden som kritisk element6 og tæt samarbejde med højt specialiseret enhed/neurokirurger.
Formålet med denne vejledning er at sikre ensartet neuroprotektiv behandling til patienten med potentielt forhøjet ICP. Fokus er 1) at erkende at der potentielt er forhøjet ICP, 2) undgå at forværre/udløse tilstanden og 3) hurtigst muligt konferere patienten med højt specialiseret enhed med henblik på at behandle den tilgrundliggende årsag og eventuel ICP-monitorering.
Målgruppen for denne vejledning er den almene intensivlæge/anæstesiolog som modtager/behandler kritisk syge. Gruppen af patienter med potentielt forhøjet ICP er heterogen. Vejledningen er tænkt som en praktisk, generel vejledning og ikke en gennemgang af de enkelte sygdomsgrupper. Her henvises til højt specialiseret enhed.
Patient med potentielt forhøjet ICP
Flere typer kritisk syge patienter kan have forhøjet ICP (Tabel 1)
Tabel 1. Eksempler på patienter med potentielt forhøjet ICP

Kliniske tegn på forhøjet ICP, såsom ændret bevidsthedsniveau, hovedpine og kvalme (Tabel 2), kan være vanskelige at erkende hos den kritisk syge patient pga. analgetica, sedation, intubation, sepsis mm. CT-C kan give mistanke om forhøjet ICP og årsager til dette. Dog kan forhøjet ICP ikke erkendes uden en ICP-måler 45. Dvs. der kan være forhøjet ICP ved en normal CTC 45. Derfor skal der være en høj grad af mistanke til forhøjet ICP hos disse patienter og faktorer som kan forværre tilstanden undgås fx hypotension, hyponatriæmi og insufficient analgo-sedation ved procedure og transport.38-11. Omvendt skal der ikke overbehandles og andre årsager overvejes/behandles. Hurtigst mulig konference med højt specialiseret enhed er afgørende med henblik på at behandle årsagen til forhøjet ICP og eventuel overflytning til ICP-monitorering/behandling 6. Indikationen for ICP-måler og kirurgisk intervention stilles af neurokirurg. Det afgørende er at neurokirurgen skal spørges og oplyses om faktorer, der taler for eventuel ICP-monitorering (f.eks. sedation, behov for dialyse m.m.) og imod (f.eks. svær koagulopati) for at kunne tage stilling og for at kunne iværksætte tidskritisk behandling. Der skelnes mellem tilstande med truende inkarceration som er akut livstruende og forhøjet ICP (Tabel 2).
Tabel 2. Kliniske tegn på forhøjet ICP og truende inkarceration

Faktorer af betydning for ICP og CPP
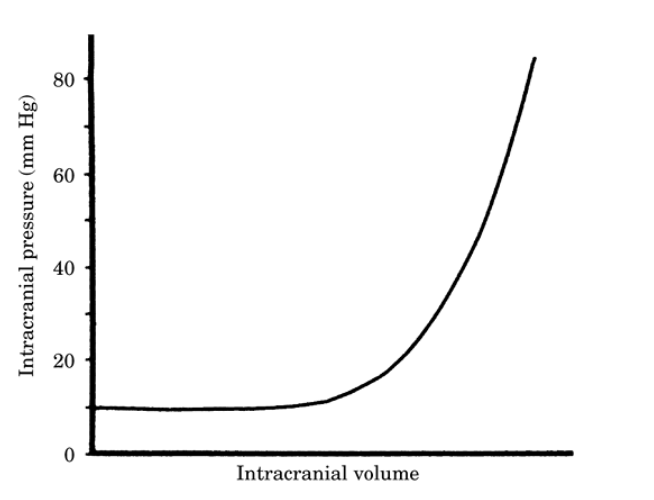
Kraniekassen indeholder cerebrospinalvæske (CSF), blod og hjernevæv. Øges volumen – af en eller flere komponenter uden tilsvarende reduktion af andre – stiger ICP (Monroe-Kellie doktrinen). Dette er illustreret ved tryk-volumenkurven, figur 1.
Figur 1. Tryk-volumenkurven
Faktorer som kan øge ICP
- Rumopfyldende proces: Blødning, tumor, ødem, absces, hydrocephalus
- paCO2-øgning → Cerebral vasodilatation
- Nedsat venøst afløb: Obstruktion af flow på hals (tryk, stiv halskrave, drejet/flekteret nakke), lejring fladt/trendelenburg/bugleje, højt PEEP, APRV
- Nedsat MAP → Cerebral vasodilatation ved intakt autoregulation
- P-Na-fald → Øger hjernevand/hævelse af hjernen
- Utilstrækkelig CSF drænage: Hydrocephalus, malfungerende EVD/IVD
- Høj kropstemperatur
- Stress ved procedure: Særligt intubation, bronkoskopi, transport, forflytning8
- Utilstrækkelig analgo-sedation/manglende muskelrelaxation ved procedure
- Svær hypertension, højt CPP (aldersafhængigt)
- Hypertension ved ophævet autoregulation
- Dialyse (Dialyse disequilibrium syndrome)12
Faktorer som kan reducere ICP13
- Analgosedation14
- paCO2-reduktion → Cerebral vasokonstriktion
- Optimalt venøst afløb: Hovedgærdet eleveret og hovedet i neutralstilling
- Øget MAP i området 60-160 mmHg hos voksne → Vasokonstriktion ved intakt autoregulation
- P-Na-øgning → Reduktion af hjernevand/skrumpning af hjernen – Muskelrelaxation9
- Temperaturkontrol
- CSF drænage: EVD, IVD, frakturer i kraniekassen
- Kirurgisk fjernelse af rumopfyldende proces: Hæmatom, tumor, cerebral absces
- Kraniektomi
Cerebralt perfusionstryk CPP og MAP
Udover forhøjet ICP i sig selv, er tilstrækkeligt CPP (CPP = MAP – ICP) afgørende for at undgå cerebral iskæmi.136. Da patienten ikke har ICP-måler sikres hos voksne med potentielt forhøjet ICP et MAP på 80 mmHg, så et ICP på 20 mmHg vil resultere i et CPP på 60 mmHg. 1115 Hos børn sikres MAP på højeste percentil svarende til alder 16. Den højere MAP-grænse holdes til forhøjet ICP kan udelukkes og/eller monitoreres, f.eks. ved opvågning eller ICP-monitorering.
Neuroprotektiv ABCD-behandling af patient med potentielt forhøjet ICP
A Sikre luftvej:
- Ved GCS 3-8 og/eller hastigt fald i GCS (oftest intubation1)
- Neuroprotektiv intubation: Tilstrækkelig anæstesi og muskelrelaxation for at undgå ICP stigning, samtidig skal blodtryksfald undgås vha. sympatometika
B Ventilation:
- Sikre paO2 10–12 kPa
- Sikre paCO2 4.5 til 5.5 kPa (om muligt anvendes end tidal CO2-monitorering)
C Cirkulation:
- Sikre MAP 80 mmHg hos voksne og børn ældre end 12 år15/li>
- Sikre aldersafhængigt MAP hos børn (1 år: MAP 55, 2–12 år: MAP 55 + 1.5 x alder)16
- Ved kliniske tegn til hypovolæmi udredes årsag og korrigeres evt. med iv bolus 0.9% NaCl: 1517Voksne 10 ml/kg og børn 10-20 ml/kg. Vurder effekt. Hvis der ikke er tegn til hypovolæmi øges MAP med noradrenalin
- Prioritér arteriekanyle, om muligt før evt. intubation
- Ved svær hypertension (MAP voksne > 130–140 mm Hg, hos børn aldersafhængigt) skal overvejes cerebral forværring og evt. CT-C og punkter under D gennemgås inden evt. sænkning af blodtryk D Disability:
- Optimal lejring: Hovedet i neutral stilling og hovedgærdet eleveret 10–15°. Obs. Cervikal columna fraktur ved samtidigt traume. Overvej at udskifte stiv halskrave med sandsække og at fjerne hovedpuden
- Sikre sufficient sedation og analgesi. Dette gælder særligt ved procedurer som bronkoskopi og transport (til CTC eller andet hospital) som kan øge stress og derved ICP
D Disability:
- Optimal lejring: Hovedet i neutral stilling og hovedgærdet eleveret 10–15°. Obs. Cervikal columna fraktur ved samtidigt traume. Overvej at udskifte stiv halskrave med sandsække og at fjerne hovedpuden
- Sikre sufficient sedation og analgesi. Dette gælder særligt ved procedurer som bronkoskopi og transport (til CTC eller andet hospital) som kan øge stress og derved ICP
- P-Na 137–144 mmol/l. 17 Undgå selv mindre fald i P-Na (fx ~ 4 mmol/l). Derfor er 0.9% NaCl førstevalg og der gives som udgangspunkt ikke hypotone iv væsker som Ringerlaktat/acetat, 18 5% glukose og Darrow-glukose. 10 Hypotone opløsninger anvendes ej heller til opblanding af medicin f.eks. NAC-drop eller remifentanil. o Ved fald i P-Na (akut A-gas) øges P-Na vha. iv bolus 1 mmol/kg hyperton NaCl o Ved truende inkarceration iv bolus 2 mmol/kg hyperton NaCl
- Blodsukker 6–10 mmol/l. Ved behov for glukose iv (f.eks. små børn, akut leversvigt) anvendes som udgangspunkt færdigblandet 0.9% NaCl med 5% glukose eller 50% glukose for at undgå fald i P-Na • Overvej muskelrelaxation ved procedurer særligt bronkoskopi og transport89
- Lumbalpunktur kan udløse inkarceration og udføres ikke ved mistanke om truende inkarceration19
- Hvis bevidsthedsniveauet ikke kan vurderes ved klinisk undersøgelse, kan der være indikation for ICP-monitorering (se næste afsnit vedrørende indikationer)
- Monitorér med GCS eller FOUR score (Tabel 3)2021
- Ved tegn til cerebral forværring overvejes CT-C og/eller konference med højt specialiseret enhed vedr. tiltag, indikation for ICP-monitorering og evt. overflytning til specialiseret enhed
Potentielt reversible årsager til påvirket bevidsthedsniveau overvejes og behandles altid (fx hypoglykæmi, hyponatriæmi, forgiftning og meningitis).
Indikationer for akut CT cerebrum
CT-C rekvireres ved mistanke om cerebral forværring fx
- fald i GCS på 2 eller derover
- ændrede pupilforhold
- motorisk forværring
- nyopståede kramper
- blodtryksstigning/bradykardi uden anden forklaring
Intrakranielle læsioner kan ændres betydeligt i størrelse, før der sker nogen væsentlig stigning i ICP. Kombinationen af klinisk og paraklinisk monitorering, herunder regelmæssige CT-skanninger, er den bedste måde at vurdere den intrakranielle tilstand på. OBS der kan være forhøjet ICP ved en normal CTC. 45
Indikationer for anlæggelse af ICP-måler
Generelt er der indikation for ICP-monitorering ved høj sandsynlighed for forhøjet ICP, hvor bevidsthedsniveau ikke kan vurderes ud fra objektiv undersøgelse som vanligt. Det kan være pga. skaden i sig selv eller sedation. Det kan fx være:
- Ved intrakraniel infektion – særligt meningitis – med behov for intubation/sedation pga. GCS 3- 8 eller hastigt faldende GCS. 4522
- Ved hovedtraume med behov for intubation/sedation pga. GCS 3-8 eller hastigt faldende GCS
- Patient, der er intuberet/sederet/GCS 3-8 og i risiko for forhøjet ICP ved behov for dialyse (risiko for forværring pga. dialyse disequilibrium syndrom)12
Indikationen for ICP-måler stilles af neurokirurg. Det er imidlertid behandlingsansvarlig læge som adviserer neurokirurgen om, at der er en patient med potentielt behov for udvidet monitorering.
Begrænsninger
Formålet er en generel, praktisk vejledning til den kritisk syge patient, hvor fokus er at erkende at patienten kan have forhøjet ICP, undgå at forværre dette og at konferere med højt specialiseret afdeling hurtigst muligt. Derfor er ikke medtaget særlige forhold ved forskellige sygdomsgrupper, der forårsager forhøjet ICP. Der er heller ikke medtaget anbefaling om temperatur, da det kan variere mellem patientkategorier.23 Der er ingen særlig anbefaling af hæmoglobingrænser. Da der endvidere er tale om et lille volumen af patienter til den enkelte intensivlæge/anæstesiolog er der heller ikke i nærværende udgave lavet anbefaling vedrørende transkraniel doppler eller UL af optical nerve sheath til vurdering af flow/ICP forhold. Slutteligt er der lavet meget få randomiserede studier på området. Derfor bygger vejledningen på konsensus og med størst vægt på erkendelse og at undgå iatrogen forværring.
Four Score Tabel 3
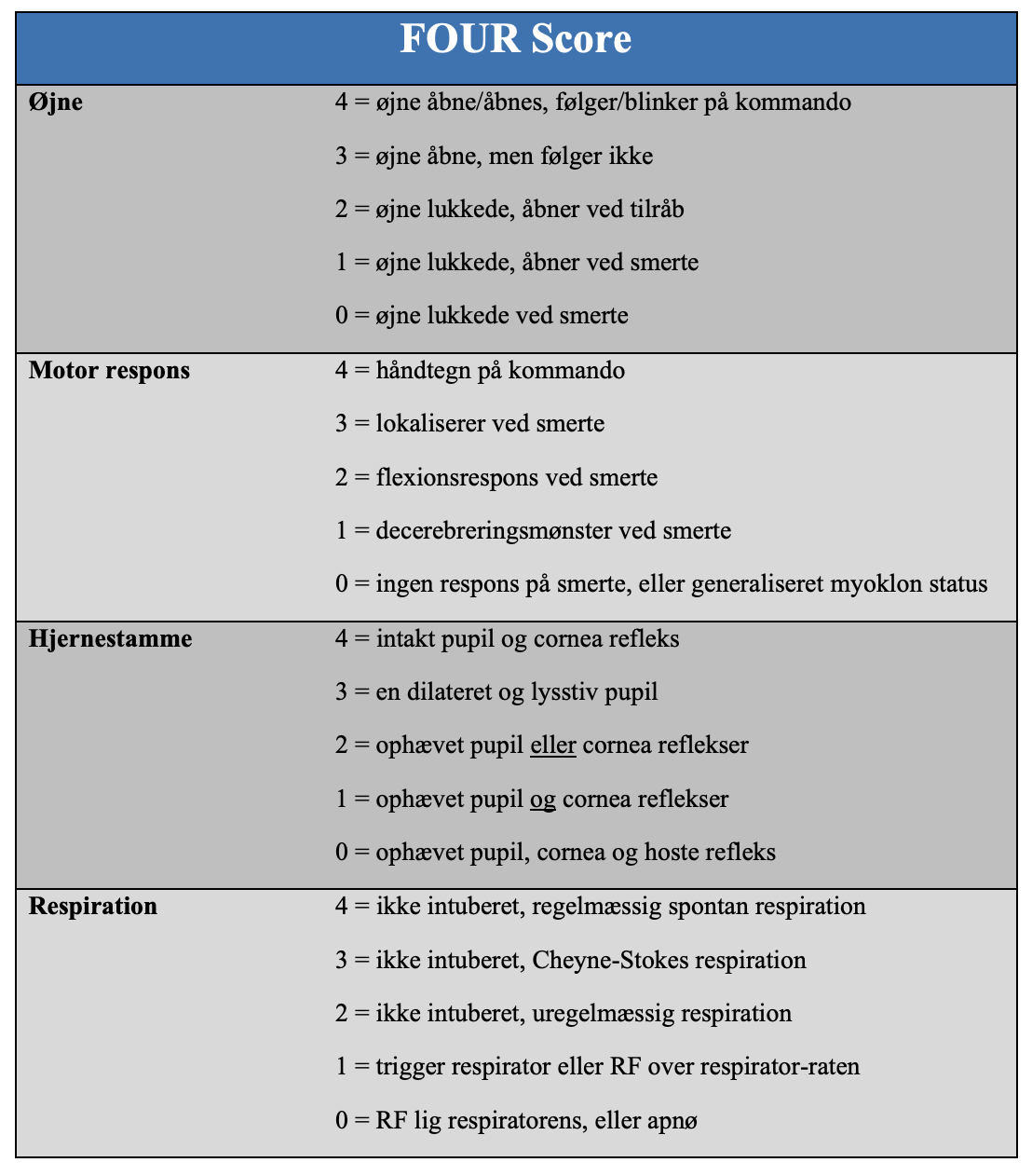
FOUR score er et alternativ til GCS til vurdering af den bevidsthedspåvirkede patient.2021 Fordelen ved FOUR score er at den inkluderer hjernestammereflekser, kan anvendes på den intuberede patient og ikke alene er udviklet til hovedtraumer. Ulempen er at den ikke er så udbredt som GCS.
Referencer
- Balestreri M, Czosnyka M, Hutchinson P, et al. Impact of intracranial pressure and cerebral perfusion pressure on severe disability and mortality after head injury. Neurocrit Care 2006;4(1):8-13. doi: 10.1385/NCC:4:1:008 [published Online First: 2006/02/25]
- Badri S, Chen J, Barber J, et al. Mortality and long-term functional outcome associated with intracranial pressure after traumatic brain injury. Intensive Care Med 2012;38(11):1800-9. doi: 10.1007/s00134- 012-2655-4 [published Online First: 2012/09/27]
- Helbok R, Olson DM, Le Roux PD, et al. Intracranial pressure and cerebral perfusion pressure monitoring in non-TBI patients: special considerations. Neurocrit Care 2014;21 Suppl 2:S85-94. doi: 10.1007/s12028- 014-0040-6 [published Online First: 2014/09/12]
- Winkler F, Kastenbauer S, Yousry TA, et al. Discrepancies between brain CT imaging and severely raised intracranial pressure proven by ventriculostomy in adults with pneumococcal meningitis. J Neurol 2002;249(9):1292-7. doi: 10.1007/s00415-002-0844-8 [published Online First: 2002/09/21]
- Larsen L, Poulsen FR, Nielsen TH, et al. Use of intracranial pressure monitoring in bacterial meningitis: a 10- year follow up on outcome and intracranial pressure versus head CT scans. Infect Dis (Lond) 2017;49(5):356-64. doi: 10.1080/23744235.2016.1269265 [published Online First: 2017/01/05]
- Guiza F, Depreitere B, Piper I, et al. Visualizing the pressure and time burden of intracranial hypertension in adult and paediatric traumatic brain injury. Intensive Care Med 2015;41(6):1067-76. doi: 10.1007/s00134-015-3806-1 [published Online First: 2015/04/22]
- Morimoto Y, Kemmotsu O, Kitami K, et al. Acute brain swelling after out-of-hospital cardiac arrest: pathogenesis and outcome. Crit Care Med 1993;21(1):104-10. doi: 10.1097/00003246-199301000- 00020 [published Online First: 1993/01/01]
- Kerwin AJ, Croce MA, Timmons SD, et al. Effects of fiberoptic bronchoscopy on intracranial pressure in patients with brain injury: a prospective clinical study. J Trauma 2000;48(5):878-82; discussion 82-3. doi: 10.1097/00005373-200005000-00011 [published Online First: 2000/05/24]
- Sanfilippo F, Santonocito C, Veenith T, et al. The role of neuromuscular blockade in patients with traumatic brain injury: a systematic review. Neurocrit Care 2015;22(2):325-34. doi: 10.1007/s12028-014-0061-1 [published Online First: 2014/09/04]
- Lunoe M, Overgaard-Steensen C. Prevention of hospital-acquired hyponatraemia: individualised fluid therapy. Acta Anaesthesiol Scand 2015;59(8):975-85. doi: 10.1111/aas.12522 [published Online First: 2015/05/12]
- Stevens RD, Shoykhet M, Cadena R. Emergency Neurological Life Support: Intracranial Hypertension and Herniation. Neurocrit Care 2015;23 Suppl 2:S76-82. doi: 10.1007/s12028-015-0168-z [published Online First: 2015/10/07]
- Esnault P, Lacroix G, Cungi PJ, et al. Dialysis disequilibrium syndrome in neurointensive care unit: the benefit of intracranial pressure monitoring. Crit Care 2012;16(6):472. doi: 10.1186/cc11877 [published Online First: 2013/01/03]
- Stocchetti N, Maas AI. Traumatic intracranial hypertension. N Engl J Med 2014;370(22):2121-30. doi: 10.1056/NEJMra1208708 [published Online First: 2014/05/30]
- Oddo M, Crippa IA, Mehta S, et al. Optimizing sedation in patients with acute brain injury. Crit Care 2016;20(1):128. doi: 10.1186/s13054-016-1294-5 [published Online First: 2016/05/06]
- Garvin R, Mangat HS. Emergency Neurological Life Support: Severe Traumatic Brain Injury. Neurocrit Care 2017;27(Suppl 1):159-69. doi: 10.1007/s12028-017-0461-0 [published Online First: 2017/09/16]
- European Paediatric Advanced Life Support (4th edition). 4 ed. Niel, Belgium: European Resuscitation Council 2016.
- Oddo M, Poole D, Helbok R, et al. Fluid therapy in neurointensive care patients: ESICM consensus and clinical practice recommendations. Intensive Care Med 2018;44(4):449-63. doi: 10.1007/s00134-018- 5086-z [published Online First: 2018/03/04]
- Rowell SE, Fair KA, Barbosa RR, et al. The Impact of Pre-Hospital Administration of Lactated Ringer’s Solution versus Normal Saline in Patients with Traumatic Brain Injury. J Neurotrauma 2016;33(11):1054-9. doi: 10.1089/neu.2014.3478 [published Online First: 2016/02/26]
- van de Beek D, Cabellos C, Dzupova O, et al. ESCMID guideline: diagnosis and treatment of acute bacterial meningitis. Clin Microbiol Infect 2016;22 Suppl 3:S37-62. doi: 10.1016/j.cmi.2016.01.007 [published Online First: 2016/04/12]
- Wijdicks EF, Bamlet WR, Maramattom BV, et al. Validation of a new coma scale: The FOUR score. Ann Neurol 2005;58(4):585-93. doi: 10.1002/ana.20611 [published Online First: 2005/09/24]
- Sharshar T, Citerio G, Andrews PJ, et al. Neurological examination of critically ill patients: a pragmatic approach. Report of an ESICM expert panel. Intensive Care Med 2014;40(4):484-95. doi: 10.1007/s00134-014-3214-y [published Online First: 2014/02/14]
- Glimaker M, Johansson B, Halldorsdottir H, et al. Neuro-intensive treatment targeting intracranial hypertension improves outcome in severe bacterial meningitis: an intervention-control study. PLoS One 2014;9(3):e91976. doi: 10.1371/journal.pone.0091976 [published Online First: 2014/03/29]
- Saxena M, Young P, Pilcher D, et al. Early temperature and mortality in critically ill patients with acute neurological diseases: trauma and stroke differ from infection. Intensive Care Med 2015;41(5):823-32. doi: 10.1007/s00134-015-3676-6 [published Online First: 2015/02/04]
Indholdsfortegenelse
